中国科学家揭示外源核酸诱导的原核生物短Ago蛋白系统发挥功能的分子机理
中国网/中国发展门户网讯 中国科学院物理研究所/北京凝聚态物理国家研究中心丁玮团队和朱洪涛团队与中国医学科学院北京协和医学院病原生物研究所崔胜团队合作,通过高分辨冷冻电镜技术与自主研发的自动化结构解析策略,在数百万计的冷冻电镜蛋白质颗粒中,高效地筛选并重构了与原核短Ago系统相关的高分辨率三维蛋白结构,并以此结构为基础结合体外功能实验,彻底揭示了原核短Argonaute(Ago)系统在病毒入侵前后所发生的结构变化。该研究成果北京时间2023年10月2日在国际学术期刊《自然》(Nature)在线发表。
核糖核酸诱导的转录后基因调控在生命个体抵御外源入侵的过程中起到至关重要的作用。自然界中的生命体无时无刻都需要应对各种外部入侵,如细菌、病毒等。为了应对这些入侵,生命体的细胞会产生一种叫做核糖核酸的分子。这些核糖核酸分子可以通过一种叫做转录后基因调控的过程,对我们的基因进行调控。我们都知道基因是我们身体内部的指令,它们决定了我们长什么样、如何工作等等。通过转录后基因调控,核糖核酸分子可以激活特定的基因,使细胞产生抗体或其他防御机制来对抗入侵者。因此,核糖核酸诱导的转录后基因调控在我们身体的免疫系统中起着非常重要的作用,可以帮助我们抵御外部入侵,并保护我们的健康。
Ago蛋白便是一种能够接受外源核酸诱导并行使防御机制对抗入侵者的功能载体。Ago蛋白存在于古菌、细菌和真核生物等生命体中,它为非编码小核糖核酸提供锚位点,达到降解靶基因或者抑制翻译的目的。在生命体健康的情况下,Ago蛋白会以个体的形式在生命体内游弋。当检测到病毒的核酸入侵时,它们会迅速组合成功能单位,迅速分解体内的辅酶I(NAD+,即烟酰胺腺嘌呤二核苷酸)。辅酶I是负责传递氢离子的辅酶,参与生命体内的糖酵解、呼吸链等生命活动。它的大量消耗意味着被病毒感染的生命体会迅速走向死亡。而随着宿主的死去,入侵的病毒同样无法继续生存,从而不可能继续复制再去侵染其他的生命体。早在20世纪50年代,科学家们就通过间接的手段检测到了生命体内存在着这种同归于尽的自我保护行为,但受限于当时的软硬件水平,这一过程的实现机制,一直是困扰科学家们的谜题。
该研究通过高分辨冷冻电镜技术与自主研发的自动化结构解析策略,在数百万计的冷冻电镜蛋白质颗粒中,高效地筛选并重构了与原核短Ago系统相关的高分辨率三维蛋白结构,并以此结构为基础结合体外功能实验,彻底揭示了原核短Ago系统在病毒入侵前后所发生的结构变化【图1b-f】。
当病毒入侵发生时,原核短Ago系统功能单元单体会从入侵基因的转录组中获得引导核糖核酸片段。该引导核糖核酸片段会与原核短Ago系统结合,并进一步通过碱基配对识别与引导核糖核酸序列互补的目标脱氧核糖核酸 【图1b-c】。在此过程中,引导核糖核酸可能会从它在MID结构域中的结合位点上解离,以便引导核糖核酸与靶向脱氧核糖核酸的杂交双链的形成。杂交双链的形成会导致原核短Ago系统的构象发生变化,并通过MID结构域形成二聚体【图1c】。而在形成二聚体的过程中,一个功能单元的TIR结构域会发生翻转并与另一个功能单元的TIR相互作用,使得两个TIR结构域以头尾相接的形式组织在一起,并在作用界面上形成一个完整的降解辅酶I的活性位点【图1d】。最后,两个二聚体会进一步通过它们的TIR结构域形成一个四聚体【图1e】。四聚体形式的组装体能够起到降解辅酶I的作用。而生命体内辅酶I的快速耗尽,将导致生命体本身的死亡,从而阻止了入侵病毒的进一步扩增。这项工作对于深入理解原核短Ago系统如何发挥功能提供了重要的结构基础,同时也最终揭示了原核短Ago中降解辅酶I的激活机制以及导致细菌等生命体死亡的分子机理【图2】,为后续对人体免疫系统的研究以及相关药物的研发提供了结构基础和理论指导。
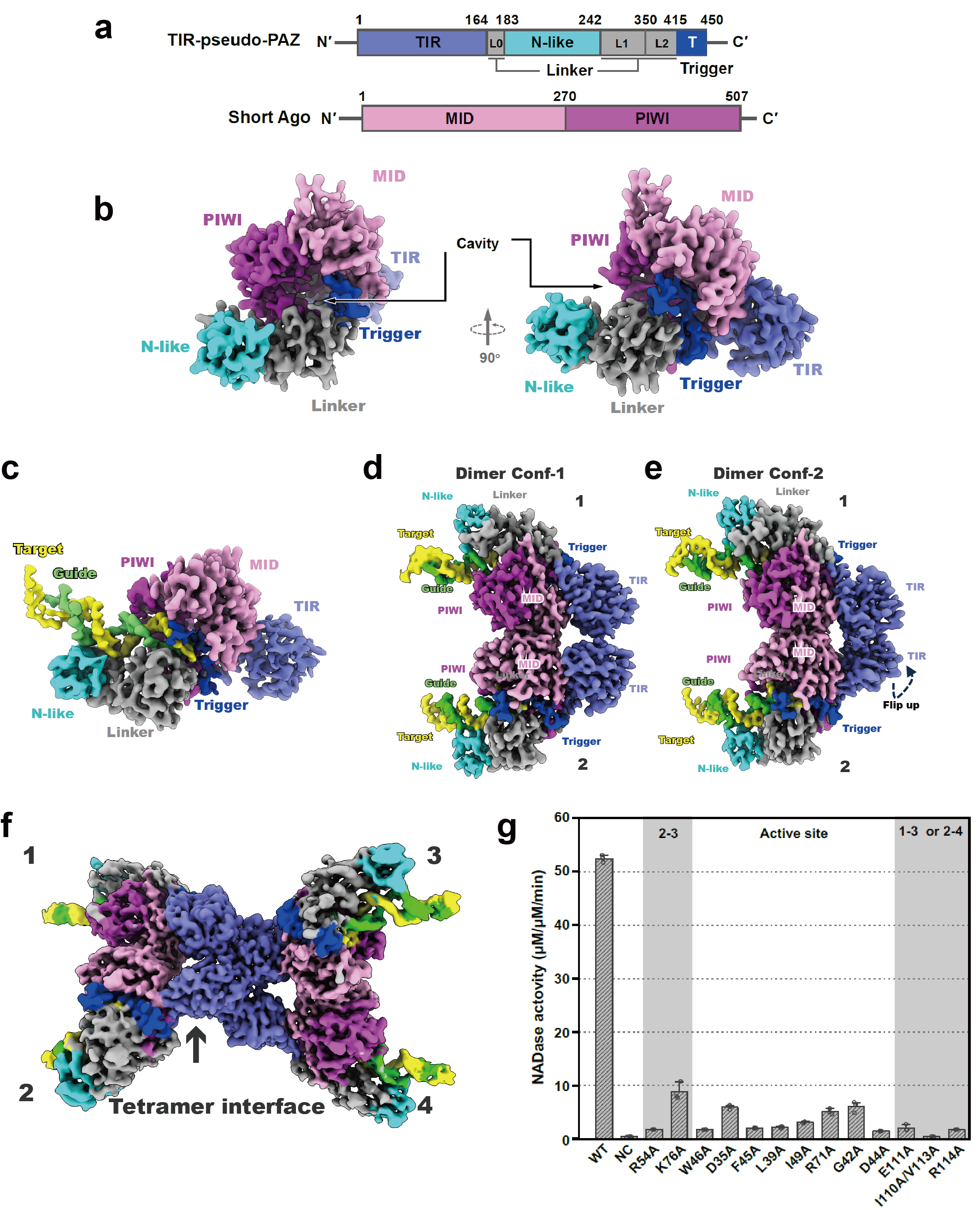
【图1】原核短Ago的三维高分辨结构
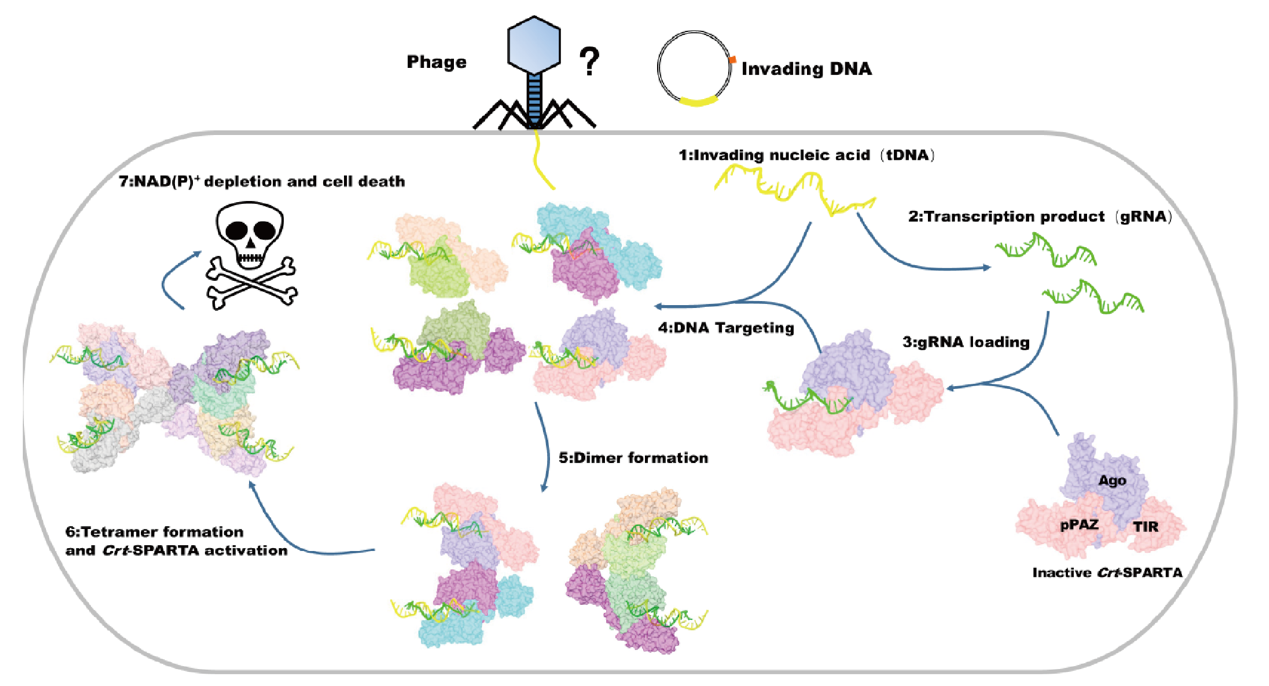
【图2】原核短Ago中辅酶I的激活机制以及导致细菌死亡的分子机理












